
Back سيستين Arabic سیستین AZB Цыстын Byelorussian Цистин Bulgarian Cistin BS Cistina Catalan Cystin German Κυστίνη Greek Cystine English Cistino Esperanto
| Cistina | |
|---|---|
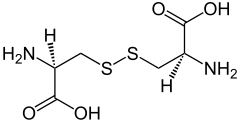 | |
| Nome IUPAC | |
| acido (2R,7R)-3,3'-ditiobis(2-amminopropanoico) | |
| Nomi alternativi | |
| L-(–)-Cistina (2S,7S)-(–)-Cistine Dicisteina | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H12N2O4S2 |
| Massa molecolare (u) | 240,29 |
| Aspetto | Solido cristallino bianco |
| Numero CAS | |
| Numero EINECS | 200-296-3 |
| PubChem | 67678 e 6992103 |
| DrugBank | DBDB00138 |
| SMILES | C(C(C(=O)O)N)SSCC(C(=O)O)N |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | 112 mg/L |
| Temperatura di fusione | 260-261 °C (533,15-534,15 K) |
| Indicazioni di sicurezza | |
| Frasi H | --- |
| Consigli P | ---[1] |
La cistina è un amminoacido solforato caratterizzato da formula molecolare C6H12N2O4S2 e ottenuto per reazione ossidativa di due molecole di cisteina. Si presenta come un solido incolore con punto di fusione 260-261 °C. Fu scoperta nel 1810 da William Hyde Wollaston ma fu riconosciuta come un componente delle proteine solamente quando venne isolata dalle corna di una vacca, nel 1899.
La cistina è presente in molte proteine e ne influenza significativamente la struttura terziaria. La cistina è anche parzialmente responsabile della formazione di una matrice di glutine nel pane, insieme all'instaurarsi di legami a idrogeno e interazioni idrofobiche. Questo amminoacido è significativamente presente nei peli umani, in particolare è responsabile della forma ondulata dei capelli, ondulazione dovuta alla formazione dei caratteristici ponti disolfuro (-S-S-).
- ^ Sigma Aldrich; rev. del 26.01.2011
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search