
Back Vinclo d'hidrocheno AN رابطة هيدروجينية Arabic Fuercia per ponte d'hidróxenu AST Hidrogen rabitəsi Azerbaijani Вадародная сувязь Byelorussian Водородна връзка Bulgarian হাইড্রোজেন বন্ধন Bengali/Bangla Vodikova veza BS Enllaç per pont d'hidrogen Catalan Vodíková vazba Czech

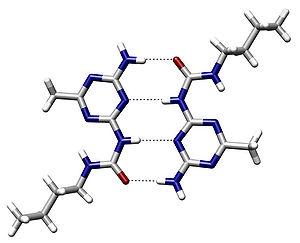


'n Waterstofbinding is 'n spesiale soort dipool-dipoolkrag wat bestaan tussen 'n elektronegatiewe atoom en 'n Waterstof atoom wat aan Stikstof, Suurstof of Fluoor verbind is. Hierdie soort verbinding behels altyd 'n waterstofatoom en die aantrekkingsenergie is by benadering omtrent so sterk soos swak kovalente verbindings (155 kJ/mol), daarom die naam – Waterstofbinding. 'n Tipiese kovalente verbinding is slegs sowat 20 keer sterker as 'n intramolekulêre waterstofbinding. Hierdie aantrekkingskragte kan tussen molekules (“intermolekulêr”) of tussen verskillende dele van dieselfde molekuul (“intramolekulêr”) voorkom.[2] Die waterstofbinding is 'n is 'n baie sterk vaste dipool-dipool van der Waals-Keesomkrag, maar swakker as kovalente-, ioniese- en metaalbindings. Die sterkte van waterstofbinding lê iewers tussen kovalente- en elektrostatiese intermolekulêre aantrekkingskragte.
Intermolekulêre waterstofbinding is verantwoordelik vir die hoë kookpunt van water (100 °C). Intramolekulêre waterstofbinding is deels verantwoordelik vir die sekondêre, tertiêre en kwarternêre strukture van proteïene en nukleoonsure
- ↑ Felix H. Beijer, Huub Kooijman, Anthony L. Spek, Rint P. Sijbesma, E. W. Meijer (1998). "Self-Complementarity Achieved through Quadruple Hydrogen Bonding". Angew. Chem. Int. Ed. 37: 75–78. doi:10.1002/(SICI)1521-3773(19980202)37:1/2%3C75::AID-ANIE75%3E3.0.CO;2-R.
{{cite journal}}: AS1-onderhoud: meer as een naam (link) - ↑ Nic, M.; Jirat, J.; Kosata, B., reds. (2006–). "hydrogen bond". IUPAC Compendium of Chemical Terminology (Aanlyn uitg.). doi:10.1351/goldbook.H02899. ISBN 0-9678550-9-8.
{{cite book}}: Gaan datum na in:|year=(hulp); Onbekende parameter|chapterurl=geïgnoreer (hulp)
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search