Back Rutenium Afrikaans ሩቴኒየም Amharic Rutenio AN रूथेनियम ANP روثينيوم Arabic روثينيوم ARY روثينيوم ARZ Ruteniu AST Rutel AVK Rutenium Azerbaijani
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ruthenium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pronunciation | /ruːˈθiːniəm/ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Appearance | silvery white metallic | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standard atomic weight Ar°(Ru) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ruthenium in the periodic table | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic number (Z) | 44 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Group | group 8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Period | period 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Block | d-block | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electron configuration | [Kr] 4d7 5s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrons per shell | 2, 8, 18, 15, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physical properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phase at STP | solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting point | 2607 K (2334 °C, 4233 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Boiling point | 4423 K (4150 °C, 7502 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Density (at 20° C) | 12.364 g/cm3[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| when liquid (at m.p.) | 10.65 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Heat of fusion | 38.59 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Heat of vaporization | 619 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar heat capacity | 24.06 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Vapor pressure
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidation states | common: +3, +4 −2,[4] 0,[5] +1,[4] +2,[4] +5,[4] +6,[4] +7,[4] +8[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativity | Pauling scale: 2.2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionization energies |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic radius | empirical: 134 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Covalent radius | 146±7 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Other properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Natural occurrence | primordial | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
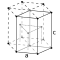
| Crystal structure | hexagonal close-packed (hcp) (hP2) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lattice constants | a = 270.58 pm c = 428.16 pm (at 20 °C)[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal expansion | 6.78×10−6/K (at 20 °C)[3][a] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermal conductivity | 117
αa 5.77 αc 8.80 αavr 6.78 W/(m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrical resistivity | 71 nΩ⋅m (at 0 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetic ordering | paramagnetic[6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molar magnetic susceptibility | +39×10−6 cm3/mol (298 K)[6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Young's modulus | 447 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Shear modulus | 173 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bulk modulus | 220 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Speed of sound thin rod | 5970 m/s (at 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poisson ratio | 0.30 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohs hardness | 6.5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinell hardness | 2160 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS Number | 7440-18-8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| History | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Naming | from Latin Ruthenia for Russia[7][8] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Discovery and first isolation | Karl Ernst Claus (1844) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopes of ruthenium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ruthenium is a chemical element; it has symbol Ru and atomic number 44. It is a rare transition metal belonging to the platinum group of the periodic table. Like the other metals of the platinum group, ruthenium is unreactive to most chemicals. Karl Ernst Claus, a Russian scientist of Baltic-German ancestry, discovered the element in 1844 at Kazan State University and named it in honor of Russia. (He used the Latin name Ruthenia, which can have other meanings, but specifically stated that the element was named in honor of his "motherland".) Ruthenium is usually found as a minor component of platinum ores; the annual production has risen from about 19 tonnes in 2009[10] to some 35.5 tonnes in 2017.[11] Most ruthenium produced is used in wear-resistant electrical contacts and thick-film resistors. A minor application for ruthenium is in platinum alloys and as a chemical catalyst. A new application of ruthenium is as the capping layer for extreme ultraviolet photomasks. Ruthenium is generally found in ores with the other platinum group metals in the Ural Mountains and in North and South America. Small but commercially important quantities are also found in pentlandite extracted from Sudbury, Ontario, and in pyroxenite deposits in South Africa.[12]
- ^ "Standard Atomic Weights: Ruthenium". CIAAW. 1983.
- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. (4 May 2022). "Standard atomic weights of the elements 2021 (IUPAC Technical Report)". Pure and Applied Chemistry. doi:10.1515/pac-2019-0603. ISSN 1365-3075.
- ^ a b c d Arblaster, John W. (2018). Selected Values of the Crystallographic Properties of Elements. Materials Park, Ohio: ASM International. ISBN 978-1-62708-155-9.
- ^ a b c d e f g Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. p. 28. ISBN 978-0-08-037941-8.
- ^ Ru(0) is present in the carbonyl-phosphine complex Ru(CO)2(PPh3)3, see Stephane Sentets, Maria del Carmen Rodriguez Martinez, Laure Vendier, Bruno Donnadieu, Vincent Huc, Noël Lugan, and Guy Lavigne (2005). "Instant "Base-Promoted" Generation of Roper's-type Ru(0) Complexes Ru(CO)2(PR3)3 from a Simple Carbonylchlororuthenium(II) Precursor". J. Am. Chem. Soc. 127 (42): 14554–14555. doi:10.1021/ja055066e. PMID 16231891.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ^ a b Haynes, p. 4.130
- ^ Lewis, David E. (2 September 2019). "The Minor Impurity in Spent Ores of the "Siberian Metal": Ruthenium Turns 175". Chemistry – A European Journal. 25 (49): 11394–11401. doi:10.1002/chem.201901922. ISSN 0947-6539.
- ^ Pitchkov, By V. N. (1 October 1996). "The Discovery of Ruthenium: "I Named The New Body, in Honour of my Motherland"". Platinum Metals Review. 40 (4): 181–188. doi:10.1595/003214096X404181188. ISSN 0032-1400.
- ^ Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). "The NUBASE2020 evaluation of nuclear properties" (PDF). Chinese Physics C. 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ^ "Ruthenium (summary)". Market review. platinum.matthey.com. 2009. p. 9.
- ^ "Platinum group metals (PGM) market report". Market research. platinum.matthey.com. May 2018. p. 30.
- ^ Haynes (2016), p. 4.31.
Cite error: There are <ref group=lower-alpha> tags or {{efn}} templates on this page, but the references will not show without a {{reflist|group=lower-alpha}} template or {{notelist}} template (see the help page).
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search