
Back Molekuul Afrikaans Molekül ALS ሞለኪውል Amharic Molecula AN Gemot ANG جزيء Arabic অণু Assamese Molécula AST Molekul Azerbaijani مولکول AZB



Kimikan, molekula deitzen zaio bi atomo edo gehiagoz osatuta dagoen egiturari. Atomo horiek lotura kimiko sendoen bidezko antolamendu definitua dute, elektrikoki neutroa eta aski egonkorra dena.[4][5][6][7][8][9] Kimika organikoan eta biokimikan, molekula terminoak ez dauka esanahi hain hertsia, eta, askotan, molekula organiko kargatuei eta biomolekulei ere aplikatzen zaie. Zentzu hertsian, molekulak eta ioi poliatomikoak bereiztu egiten dira.
Molekularen egitura hobeto ezagutu ahala, definizio hau aldatzen joan da. Aurreko definizioak zehazgabeagoak ziren: substantzia kimikoen konposizio eta propietate kimikoak atxikitzen zituen partikularik txikienatzat hartzen zen molekula.[10] Definizio hau sarritan ez zen betetzen, eguneroko substantzia asko (esaterako, hainbat arroka, gatz edo metal), ez baitaude molekulaz eginak.
Gasen teoria zinetikoan, molekula terminoa edozein gas-partikuletarako erabiltzen da, bere osaera kontuan hartu gabe.[11] Definizio honek badauka desabantaila bat: gas nobleak ere molekulak izango lirateke, loturarik gabeko atomo bakunez osatuta baitaude.
Molekulen antzeko kontzeptuak antzinatik eztabaidatzen dira, baina molekulen izaerari eta haien loturei buruzko ikerketa modernoa XVII. mendean hasi zen. Denborarekin, Robert Boyle, Amedeo Avogadro, Jean Perrin eta Linus Pauling moduko zientzialariek finduta, molekulen ikerketa, gaur egun, fisika molekularra edo kimika molekularra izenez ezagutzen da.
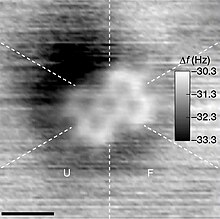
- ↑ (Ingelesez) Iwata, Kota; Yamazaki, Shiro; Mutombo, Pingo; Hapala, Prokop; Ondráček, Martin; Jelínek, Pavel; Sugimoto, Yoshiaki. (2015-07-16). «Chemical structure imaging of a single molecule by atomic force microscopy at room temperature» Nature Communications 6 (1): 7766. doi:. ISSN 2041-1723. PMID 26178193. PMC PMC4518281. (Noiz kontsultatua: 2023-06-13).
- ↑ (Ingelesez) Dinca, L. E.; Marchi, F. De; MacLeod, J. M.; Lipton-Duffin, J.; Gatti, R.; Ma, D.; Perepichka, D. F.; Rosei, F.. (2015-02-05). «Pentacene on Ni(111): room-temperature molecular packing and temperature-activated conversion to graphene» Nanoscale 7 (7): 3263–3269. doi:. ISSN 2040-3372. (Noiz kontsultatua: 2023-06-13).
- ↑ (Ingelesez) Hapala, Prokop; Švec, Martin; Stetsovych, Oleksandr; van der Heijden, Nadine J.; Ondráček, Martin; van der Lit, Joost; Mutombo, Pingo; Swart, Ingmar et al.. (2016-05-27). «Mapping the electrostatic force field of single molecules from high-resolution scanning probe images» Nature Communications 7 (1): 11560. doi:. ISSN 2041-1723. PMID 27230940. PMC PMC4894979. (Noiz kontsultatua: 2023-06-13).
- ↑ IUPAC
- ↑ Pauling, Linus. (1970). General Chemistry. New York: Dover Publications, Inc. ISBN 0-486-65622-5..
- ↑ Ebbin, Darrell, D.. (1990). General Chemistry. (3. argitaraldia) Boston: Houghton Mifflin Co. ISBN 0-395-43302-9..
- ↑ Brown, T.L.. (2003). Chemistry – the Central Science. (9. argitaraldia) New Jersey: Prentice Hall ISBN 0-13-066997-0..
- ↑ Chang, Raymond. (1998). Chemistry. (6. argitaraldia) New York: McGraw Hill ISBN 0-07-115221-0..
- ↑ Zumdahl, Steven S.. (1997). Chemistry. (4. argitaraldia) Boston: Houghton Mifflin ISBN 0-669-41794-7..
- ↑ Molekularen definizioa (Frostburg State University)
- ↑ Ikus [1]
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search