
Back حمض الهيدرازويك Arabic Hidrogen azid Azerbaijani هیدرازوئیک اسید AZB Азотоводородна киселина Bulgarian Àcid hidrazoic Catalan ترشی ھایدرازۆیک CKB Kyselina azidovodíková Czech Stickstoffwasserstoffsäure German Hydrazoic acid English Azida de hidrógeno Spanish
| |

| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Hydrogen azide
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| HN3 | |
| Massa molar | 43,03 g/mol |
| Penampilan | cairan tak berwarna, sangat mudah menguap |
| Densitas | 1,09 g/cm3 |
| Titik lebur | -80 °C |
| Titik didih | 37 °C |
| sangat mudah larut | |
| Kelarutan | larut dalam alkali, alkohol, eter |
| Keasaman (pKa) | 4,6[1] |
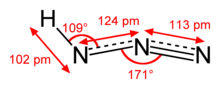
| Struktur | |
| mendekati linier | |
| Bahaya | |
| Bahaya utama | Sangat beracun, mudah meledak, reaktif |
| Frasa-R | R3, R27/28 |
| Frasa-S | S33, S36/37, S38 |
| Senyawa terkait Error in template * unknown parameter name (Template:Chembox Related): "OtherFunctn_label; OtherFunctn" (See parameter list). This message only shows in Pratayang, it will not show after Terbitkan perubahan.
| |
Kation lainnya
|
Natrium azida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Asam hidrazoat, dikenal juga sebagai hidrogen azida atau azoimida,[2] adalah suatu senyawa dengan rumus kimia HN3.[3] Ia adalah cairan tak berwarna, mudah menguap, dan mudah meledak pada suhu dan tekanan ruang. Ini merupakan senyawa nitrogen dan hidrogen, dan oleh karenanya merupakan hidrida pniktogen. Hidrogen azida pertama kali diisolasi pada tahun 1890 oleh Theodor Curtius.[4] Asam ini memiliki sedikit aplikasi, tetapi basa konjugatnya, ion azida, bermanfaat dalam proses-proses khusus.
Asam hidrazoat larut dalam air. Asam hidrazoat yang tidak diencerkan memiliki bahaya ledakan[5] dengan entalpi standar pembentukan ΔfHo (l, 298K) = +264 kJmol−1).[6] Jika diencerkan, gas dan larutan airnya (<10%) dapat ditangani dengan aman.
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^
 Chisholm, Hugh, ed. (1911). "Azoimide". Encyclopædia Britannica. 3 (edisi ke-11). Cambridge University Press.
Chisholm, Hugh, ed. (1911). "Azoimide". Encyclopædia Britannica. 3 (edisi ke-11). Cambridge University Press.
- ^ Dictionary of Inorganic and Organometallic Compounds. Chapman & Hall.
- ^ Curtius, Theodor (1890). "Ueber Stickstoffwasserstoffsäure (Azoimid) N3H". Berichte der deutschen chemischen Gesellschaft. 23 (2): 3023–3033. doi:10.1002/cber.189002302232.
- ^ Furman, David; Dubnikova, Faina; van Duin, Adri C. T.; Zeiri, Yehuda; Kosloff, Ronnie (2016-03-10). "Reactive Force Field for Liquid Hydrazoic Acid with Applications to Detonation Chemistry". The Journal of Physical Chemistry C. 120 (9): 4744–4752. doi:10.1021/acs.jpcc.5b10812. ISSN 1932-7447.
- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamaInorgChem
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search