
Back Stoigiometrie Afrikaans تكافؤ ترابط العناصر Arabic Estequiometría AST Стэхіяметрыя Byelorussian Стехиометрия Bulgarian Stehiometrija BS Estequiometria Catalan Stechiometrie Czech Støkiometri Danish Stöchiometrie German
Dalam ilmu kimia, stoikiometri (/ˌstɔɪkiˈɒmɪtri/) adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia). Kata ini berasal dari bahasa Yunani kuno στοιχεῖον stoicheion "elemen" dan μέτρον metron "pengukuran. Dalam bahasa Yunani patristik, kata Stoichiometria digunakan Nikephoros untuk merujuk pada jumlah baris dari Perjanjian Baru kanonik dan beberapa Apokrifa.
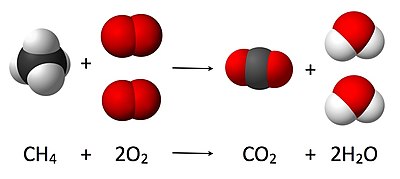
Stoikiometri didasarkan pada hukum-hukum dasar kimia, yaitu hukum kekekalan massa, hukum perbandingan tetap, dan hukum perbandingan berganda. Stoikiometri diilustrasikan melalui gambar berikut, dengan persamaan reaksi setara:
- CH4 + 2 O2 → CO2 + 2 H2O.
Di sini, satu molekul metana bereaksi dengan dua molekul gas oksigen untuk menghasilkan satu molekul karbon dioksida dan dua molekul air. Persamaan kimia khusus ini adalah contoh pembakaran sempurna. Stoikiometri mengukur hubungan kuantitatif ini, dan digunakan untuk menentukan jumlah produk dan reaktan yang diproduksi atau dibutuhkan dalam reaksi yang diberikan. Menggambarkan hubungan kuantitatif antara zat-zat ketika mereka berpartisipasi dalam reaksi kimia dikenal sebagai stoikiometri reaksi. Dalam contoh di atas, stoikiometri reaksi mengukur hubungan antara metana dan oksigen ketika mereka bereaksi membentuk karbon dioksida dan air.
Karena hubungan mol yang diketahui dengan massa atom, rasio yang diperoleh dengan stoikiometri dapat digunakan untuk menentukan jumlah massa dalam suatu reaksi yang dijelaskan oleh persamaan yang setimbang. Hal ini disebut sebagai stoikiometri komposisi.
Stoikiometri gas berkaitan dengan reaksi yang melibatkan gas, di mana gas berada pada suhu, tekanan, dan volume yang diketahui dan dapat dianggap gas ideal. Untuk gas, rasio volume idealnya sama dengan hukum gas ideal, tetapi rasio massa dari reaksi tunggal harus dihitung dari massa molekul dari reaktan dan produk. Dalam praktiknya, karena keberadaan isotop, massa molar digunakan sebagai gantinya ketika menghitung rasio massa.
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search