
Back Sitroensuur Afrikaans حمض الليمون Arabic Ácidu cítrico AST Limon turşusu Azerbaijani سیتریک اسید AZB Лімонная кіслата Byelorussian Цытрынавая кісьля BE-X-OLD Лимонена киселина Bulgarian সাইট্রিক অ্যাসিড Bengali/Bangla Limunska kiselina BS
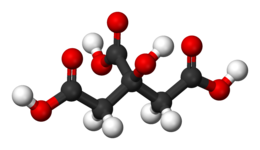
| Acido citrico | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| acido 3-carbossil-3-idrossi-1,5-pentandioico | |
| Nomi alternativi | |
| acido 2-idrossi-1,2,3-propantricarbossilico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H8O7 |
| Massa molecolare (u) | 192,12 |
| Aspetto | solido incolore |
| Numero CAS | |
| Numero EINECS | 201-069-1 |
| PubChem | 311, 19782904 e 88113319 |
| DrugBank | DBDB04272 |
| SMILES | C(C(=O)O)C(CC(=O)O)(C(=O)O)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,665 |
| Costante di dissociazione acida (pKa) a 293 K | 3,1; 4,8; 6,4 |
| Solubilità in acqua | 750 g/l a 293 K |
| Temperatura di fusione | 153 °C |
| Temperatura di ebollizione | Decompone |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −1543,8 |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 3000 mg/kg (ratto, orale) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 319 |
| Consigli P | 280 - 305+351+338 - 337+313 [1] |

L'acido citrico è un composto organico avente formula bruta C6H8O7.[2] È acido tricarbossilico solubile in acqua.
Sebbene l’acido citrico sia uno degli acidi più diffusi negli organismi vegetali ed un prodotto metabolico degli organismi aerobici, quando è solido oppure in soluzione concentrata deve essere maneggiato con cautela. Si trova in tracce nella frutta, soprattutto del genere Citrus: il succo di limone ne può contenere sino al 3-4% e l'arancia l'1%. È presente anche nei legni, nei funghi, nel tabacco, nel vino e persino nel latte.
Ogni anno vengono prodotti più di un milione di tonnellate di acido citrico. È ampiamente utilizzato come anticalcare, acidificante, acido per il restauro e chelante.[3]
I derivati dell'acido citrico vengono chiamati citrati, che comprendono sia i sali e gli esteri sia l'anione poliatomico in soluzione. Un esempio di citrato è il citrato di sodio, un esempio di estere è il trietilcitrato. È presente in piccola quantità anche in bevande zuccherate.
- ^ (EN) GESTIS Substance Database Information system on hazardous substances of the German Social Accident Insurance, Space GESTIS Substance Database - Citric acid, su gestis-en.itrust.de. URL consultato il 27 gennaio 2019 (archiviato dall'url originale l'11 novembre 2016).
- ^ (EN) PubChem, Citric Acid, su pubchem.ncbi.nlm.nih.gov. URL consultato il 6 marzo 2023.
- ^ Apelblat, Alexander,, Citric acid, ISBN 978-3-319-11232-9, OCLC 897810338.
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search