Back Etanol Afrikaans Ethanol ALS Etanol AN إيثانول Arabic ইথান'ল Assamese Etanol AST दारु AWA Etanol Azerbaijani اتانول AZB Этанол Bashkir
| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC sistematik
Ethanol[1] | |||
| Pengecam | |||
Imej model 3D Jmol
|
|||
| ECHA InfoCard | 100.000.526 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C2H6O | |||
| Jisim molar | 46.07 g·mol−1 | ||
| Ketumpatan | 0.789 g/cm3 (dalam 25°C) | ||
| Takat lebur | −114 °C (−173 °F; 159 K) | ||
| Takat didih | 78.37 °C (173.07 °F; 351.52 K) | ||
| Keasidan (pKa) | 15.9 (H2O), 29.8 (DMSO)[2][3] | ||
| Bahaya | |||
| Takat kilat | 16 °C (61 °F; 289 K) | ||
| 365 °C (689 °F; 638 K) | |||
| Dos maut (LD) atau kepekatan dos maut (LC) | |||
LD50 (median dos)
|
7060 mg/kg (oral, tikus)[4] | ||
| Sebatian berkaitan | |||
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |||
| | |||
| Rujukan kotak info | |||
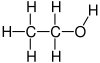
Etanol (juga dipanggil etil alkohol, alkohol bijian, alkohol minum (beer, wine, whisky, spirit), atau hanya alkohol) merupakan kandungan alkohol utama yang terkandung dalam minuman alkohol, yang dihasilkan melalui proses penapaian gula dengan menggunakan yis. Etanol mampu menyebabkan kemabukan. Selain itu, etanol juga digunakan sebagai pelarut, antiseptik, bahan api fosil dan cecair aktif dalam termometer raksa.
Etanol merupakan cecair tidak berwarna yang meruap dan mudah terbakar dengan struktur formula CH3CH2OH, yang sering disingkatkan sebagai C2H5OH atau C2H6O. Etanol juga boleh ditulis sebagai EtOH, Et merujuk kepada kumpulan etil, C2H5−.
- ^ "Ethanol – Compound Summary". The PubChem Project. USA: National Center for Biotechnology Information.
- ^ Ballinger, P., Long, F.A. (1960). "Acid Ionization Constants of Alcohols. II. Acidities of Some Substituted Methanols and Related Compounds1,2". Journal of the American Chemical Society. 82 (4): 795. doi:10.1021/ja01489a008.CS1 maint: multiple names: authors list (link)
- ^ Arnett, E.M., Venkatasubramaniam, K.G. (1983). "Thermochemical acidities in three superbase systems". J. Org. Chem. 48 (10): 1569. doi:10.1021/jo00158a001.CS1 maint: multiple names: authors list (link)
- ^ http://chem.sis.nlm.nih.gov/chemidplus/rn/64-17-5
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search